
临床案例:干细胞治疗肝病的基础和临床研究,显
纤维化通常发生在肝脏疾病的早期阶段。如果不及时治疗或控制,随着肝纤维化程度进一步恶化,最终可能发展为肝硬化甚至肝癌。 我国肝细胞癌的发病率在所有肿瘤中居第二位,而且发病率还在不断上升。
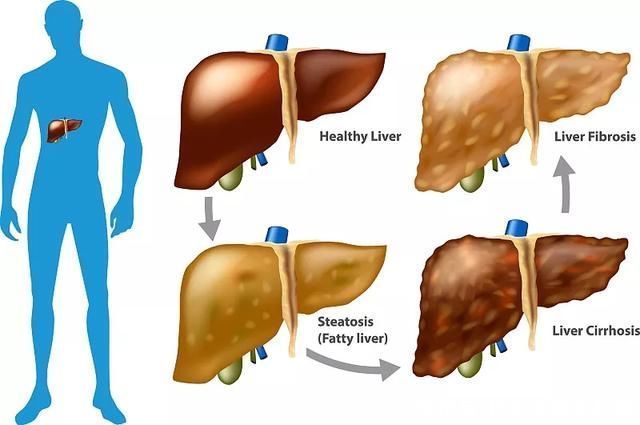
肝纤维化的形成在肝脏疾病中 主要包括肝炎病毒、酒精、自身免疫等,这些原因会引起正常肝细胞的凋亡和肝星状细胞(HSC)的活化,导致细胞外基质(ECM)在肝脏中过度积累。肝脏和肝脏结构的破坏。
传统疗法治疗肝病效果不佳
近年来肝纤维化尚无特效疗法在肝脏疾病中。一个有效的方法。对于已经发展为终末期肝病的患者,肝移植是目前最有效的治疗方法。然而,供体器官短缺、免疫排斥和高成本限制了肝移植的治疗。
用于肝病的间充质干细胞 (MSC)它被认为是一种非常有效的治疗策略。其优点是持续自我更新、增殖、多能分化和免疫调节活性,其低抗原性允许异基因 MSCs 移植。
MSCs治疗肝病的机制
MSCs诱导分化为肝细胞样细胞: MSCs移植并注射入体内后,分化为肝细胞样细胞(HLCs),这可能是MSCs移植治疗肝病的机制之一。
基础研究一: 一些研究发现,利用四氯化碳建立大鼠肝纤维化和肝硬化模型,然后输注四氯化碳人源 性交 hUC-MSCs 后,观察小鼠肝纤维化的相关指标。检测产物发现小鼠体内存在人源性ALB、AFP、CK18和CK19,但未检测到鼠源性ALB、AFP、CK18和CK19。
MSCs的免疫调节:MSCs具有免疫调节特性,通过多种方式调节机体的免疫反应。
基础研究二:Yousefifard et al.相信MSCs通过充当“转导细胞”来影响各种“效应细胞”。例如,T 细胞、B 细胞和巨噬细胞。 MSCs可以分泌多种生物活性分子,包括多种细胞因子、HGF和IL-10。 IL-10是一种免疫调节细胞因子,具有抑制血清中炎性细胞因子的作用,包括IL-6、TNF-1、干扰素-γ等,可改善肝硬化大鼠肝组织淋巴细胞的增殖,并能促进肝脏修复,抑制肝硬化的发生。
MSCs衍生的外泌体:MSCs衍生的外泌体也被认为是促进肝细胞增殖和维持肝细胞的主要机制之一功能。
基础研究三:YIN等研究证明了MSCs来源的外泌体在治疗不同疾病方面的有效性,包括缺乏症血性心脏病、肝纤维化和脑血管病。 有研究认为,输注MSCs产生的外泌体有利于促进肝损伤修复和改善肝功能。因此,他们认为MSCs分泌的生物活性细胞因子是促进肝细胞修复的主要原因。

肝干细胞治疗临床案例疾病
临床案例一:Sang et al.对包括 717 名肝硬化患者在内的 14 项试验进行了荟萃分析。证明MSCs联合中药治疗组较单纯中药治疗组有更好的治疗效果,肝功能明显改善,体现在总胆红素、丙氨酸转氨酶、凝血功能等方面。酶原时间等指标显着降低,血清白蛋白、胆碱酯酶、凝血酶原活性显着升高。
临床案例 2:Liang et al.进行了临床试验,包括26例肝硬化患者。通过外周静脉移植同种异体MSCs,包括23个脐带MSCs、2个脐带MSCs和1个骨髓MSCs。随访6个月后,总胆红素和凝血酶原时间均值下降;血清白蛋白水平升高; 6个月后,终末期肝病(MELD)评分也有所改善。
临床案例三:Fang等人进行的临床试验。表明对于失代偿期肝硬化患者,静脉移植骨髓间充质干细胞后,患者的血清白蛋白、总胆红素和凝血酶原时间得到明显改善。治疗后MSCs组Child Pugh评分也明显优于对照组,且MSCs组死亡率低于对照组。
临床案例四:有临床试验研究MSCs治疗乙型肝炎相关肝病的作用。 span>,110 名乙型肝炎相关 ACLF 患者被纳入这项开放标签、非盲法随机对照研究。
对照组(n=554)仅使用标准药物治疗(SMT);
实验组(n= 556) 输注异基因骨髓间充质干细胞4周,观察24周。
MSCs组累计存活率为73.2%; SMT 组为 55.6%。
在5~24周的随访中,MSCs输注患者没有与输注相关的副作用,但与SMT患者相比,发热更频繁。两组受试患者均未发现肿瘤。与对照组相比,异基因骨髓间充质干细胞治疗
上一篇:凭着“火眼金睛”,他为临床诊疗精准“解码”
下一篇:没有了




